



2025
、
2025
西山中科助力|艾立康药业
首个“1类创新药”
艾立康药业首款1类创新药ALK2401片获临床试验批准
西山中科提供全套研究支持,助力攻克周围神经痛
2025年9月12日 — 艾立康药业有限公司今日宣布,其全资子公司艾立康(合肥)医药科技有限公司研发的1类小分子创新药“ALK2401片”已正式获得国家药品监督管理局(NMPA)核准签发的《药物临床试验批准通知书》,批准其开展针对“周围神经病理性疼痛”的临床试验。
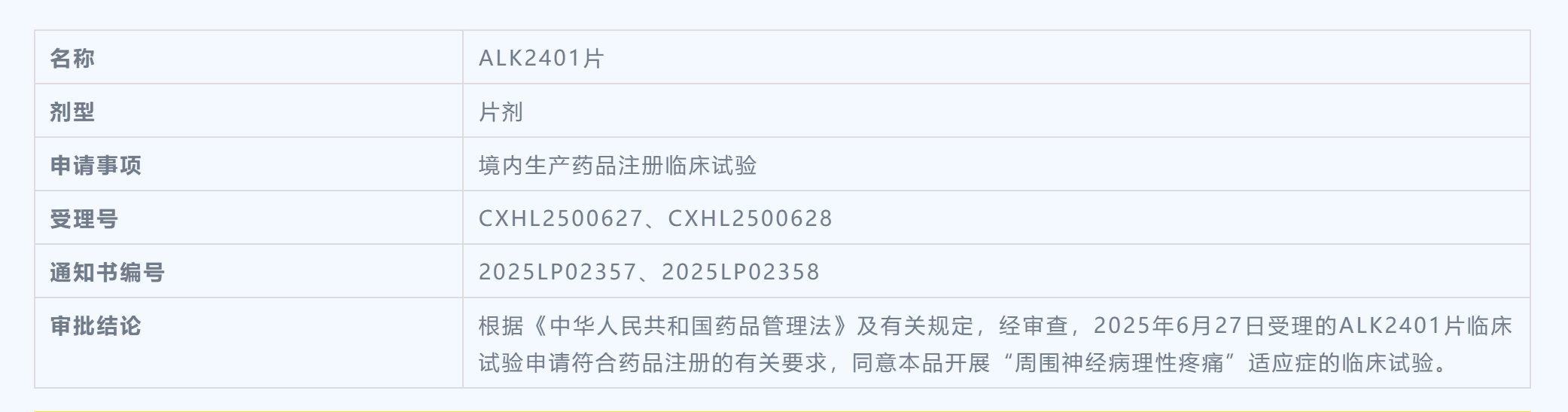
ALK2401片是一种具有全新作用机制的非阿片类、非中枢作用的选择性小分子口服抑制剂。其核心优势在于:
·全新机制:通过独特的外周镇痛机制发挥作用,可在不影响阿片类通路的情况下有效减少疼痛。
·安全性高:有效避免传统中枢镇痛药物(如阿片类药物)所带来的成瘾性、嗜睡等中枢神经系统不良反应。
·效果显著:临床前研究表明,该化合物显示出显著的镇痛效果和良好的安全性。
·市场前景广阔:有望为周围神经病理性疼痛患者提供全新的治疗选择,填补国内该靶点药物空白,并有望成为年市场规模超数十亿元的重磅创新药品种。
合作伙伴
本项目的重要合作伙伴——苏州西山中科药物研究开发有限公司——为ALK2401片提供了全套的药代动力学和毒理学研究服务,以其专业高效的一站式CRO服务平台,助力该创新药成功获批临床。
西山中科表示:“我们期待与更多的合作伙伴携手创赢,共同打造医药新未来。”
2025
信达生物制药(苏州)有限公司(以下简称“信达生物”)1类创新药玛仕度肽注射液(商品名:信尔美)获得中华人民共和国国家药品监督管理局(NMPA)批准上市。
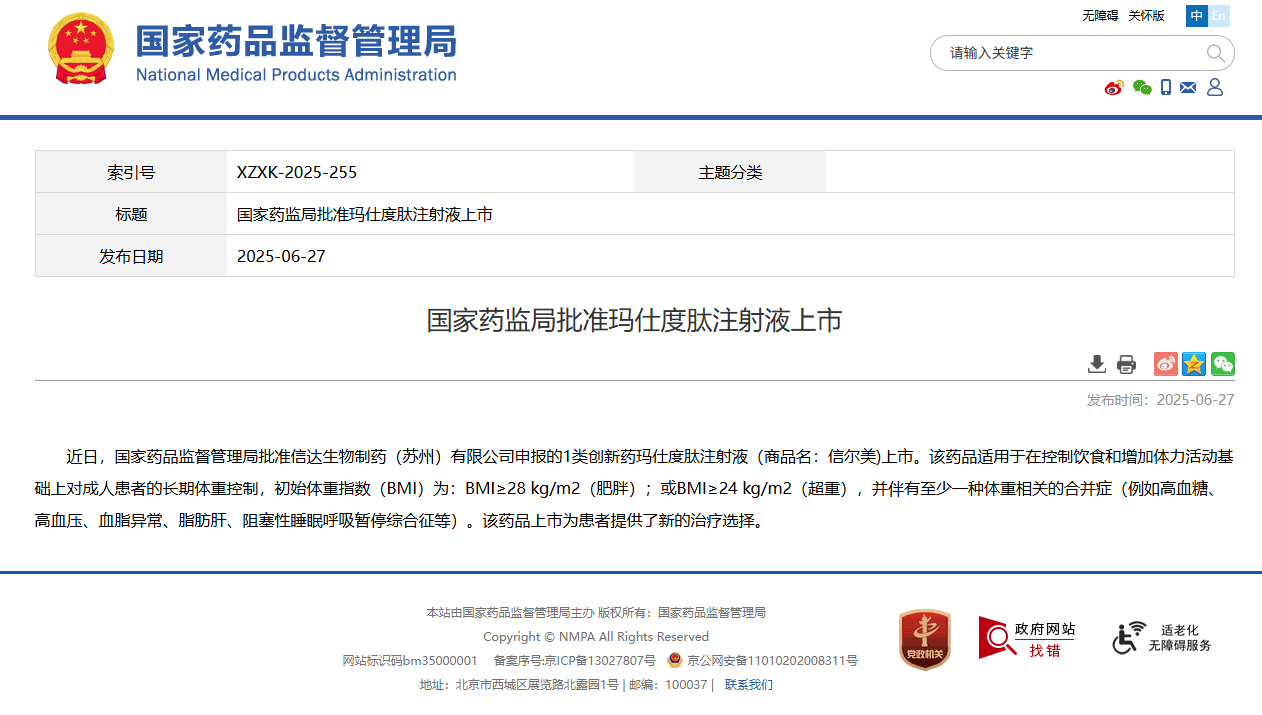
信尔美®是全球首个GCG/GLP-1双受体激动减重药物,其独特的双激动作用机制,在激动GLP-1受体抑制食欲减少热量摄入的基础上,同时激活GCG受体,促进脂肪燃烧,降低内脏脂肪含量,进一步增强玛仕度肽减重效果。临床研究表明:使用玛仕度肽体重降幅达21%,降低肝脏脂肪含量超 80%,腰围减少达11cm,颈围减少达3cm,兼顾改善血糖、血压、血脂、血尿酸和转氨酶水平等心血管及代谢指标,带来全面获益,获评2025年全球十大最受期待药物之一(FIERCE Pharma 2025),其研究成果发表于《新英格兰医学杂志》,并特配专家评述。
苏州西山中科与国辰生物联合信达生物技术团队,紧密围绕玛仕度肽注射液项目展开深度合作,依据该药物的分子特性及药品申报的严格要求,系统性地构建了一套覆盖致癌试验、生殖毒理研究等核心模块的 NDA 阶段全链条毒理学评价体系。团队严格遵循 GLP 等质量管理规范,通过科学化、标准化的研究方案设计,全面锚定药物安全性评价关键节点,为信达生物玛仕度肽注射液的临床试验获批及商业化上市提供坚实的毒理学数据支撑。
苏州西山中科药物研究开发有限公司、苏州国辰生物科技股份有限公司与信达生物制药集团将继续携手,为生物制药研发提供更优质的服务!
关于信尔美®
- 滑动查看更多介绍 -
关于信达生物
- 滑动查看更多介绍 -
2025
苏州西山中科助力银诺医药
1类新药怡诺轻®
依苏帕格鲁肽α注射液
热烈祝贺上海银诺医药技术有限公司(以下简称“上海银诺医药”)1类新药怡诺轻®(依苏帕格鲁肽α注射液)获得中华人民共和国国家药品监督管理局(NMPA)批准上市。
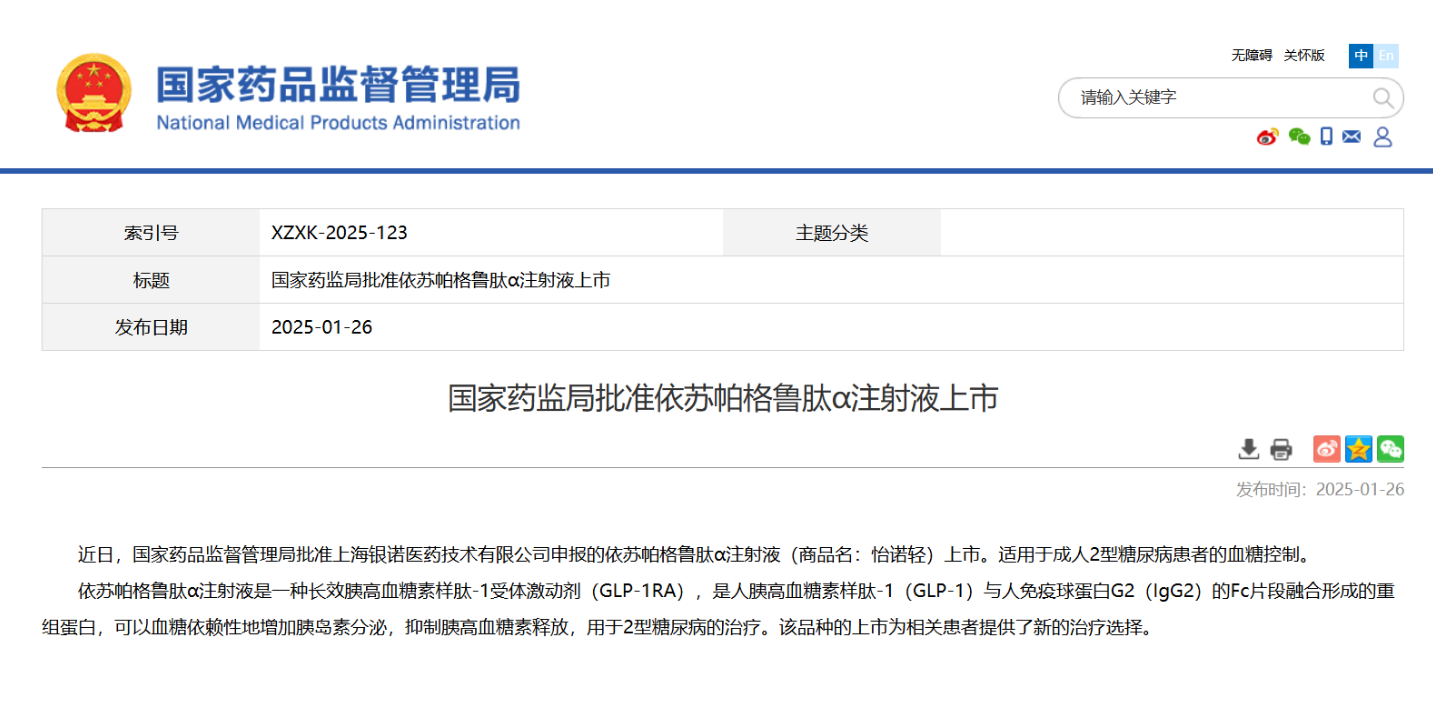
该药是一种长效胰高血糖素样肽-1受体激动剂(GLP-1RA),是人胰高血糖素样肽-1(GLP-1)与人免疫球蛋白G2(IgG2)的Fc片段融合形成的重组蛋白,可以血糖依赖性地增加胰岛素分泌,抑制胰高血糖素释放,用于2型糖尿病的治疗。该品种的上市为相关患者提供了新的治疗选择。
苏州西山中科技术团队与上海银诺医药技术团队针对该项目展开密切合作,根据依苏帕格鲁肽α注射液的特点及申报要求,科学合理地设计了包括致癌试验(大鼠、RasH2转基因小鼠)在内的系列非临床研究,严格遵循相关质量规范,全力为上海银诺依苏帕格鲁肽α注射液获批临床试验及上市保驾护航!
2024

西山中科助力超阳药业
首个1类创新药HP-001胶囊
上海超阳药业有限公司于近日收到国家药品监督管理局核准签发的关于1类创新药HP-001胶囊的《药物临床试验批准通知书》,将于近期开展临床试验,临床拟用于血液系统恶性肿瘤的治疗。

该项目临床前全套毒理试验由苏州西山中科药物研究开发有限公司承担。
超阳药业授予我公司“优秀合作伙伴”称号,以表彰公司在该项目中所提供的服务和支持。




2024
简介:”2024年05月6-10日,美国食品药品监督管理局(以下简称“FDA”)检察官员Dr. Deborah Greco、Dr. Zhou Chen和Dr. Mark Seaton对苏州西山中科药物研究开发有限公司(以下简称“苏州西山中科”)开展现场核查。“
2024年05月6-10日,美国食品药品监督管理局(以下简称“FDA”)检察官员Dr. Deborah Greco、Dr. Zhou Chen和Dr. Mark Seaton对苏州西山中科药物研究开发有限公司(以下简称“苏州西山中科”)开展现场核查。
三位检察官通过听取汇报、审查资料、现场考核等方式对公司组织机构、人员管理、设施设备、质量体系、计算机化系统等进行了全面系统的检查与评估,审核了多个研究专题,并选取多个关键试验环节进行现场考评。

各职能部门负责人及相关工作人员翘首以待,以专业、高效、诚挚的态度,迎接本次国际性核查。

检查组一致认为苏州西山中科在技术能力和质量管理等方面均符合美国FDA GLP法规要求。
本次核查的顺利通过,标志着苏州西山中科在从事新药的非临床安全性评价服务方面得到了国际上的充分认可与肯定。苏州西山中科将持续增强专业技术能力、优化质量管理,进一步提升国际化服务能力。
2024
2024年5月27日,中华人民共和国农业农村部发文公告,批准苏州西山中科药物研究开发有限公司通过农药登记试验单位认定,有效期 5年。
苏州西山中科试验范围涵盖:
1、残留试验:代谢试验(动物代谢、植物代谢);
2、毒理学试验:急性毒性试验、重复染毒毒性试验、特殊毒性试验、代谢与毒物动力学试验、微生物致病性试验、暴露量测试试验;
3、环境影响试验:生态毒理试验(A类、B类、D类)、环境归趋试验(A类、B类)。
我公司将秉持初心,一如既往做好农药登记试验服务工作,确保试验的科学性和准确性!
2023
按照党中央、省委关于主题教育部署要求和市委工作安排,今天(11月23日),区委常委、宣传部部长、统战部部长尤建丰在越溪街道开展“千村万企、千家万户”走访,深入基层、深入企业、深入群众,强服务、促发展,察民情、解民忧。他强调,要坚持以习近平新时代中国特色社会主义思想为指导,主动对接企业,问需于企、服务于企,通过实打实的举措,帮助企业解决实际困难,不断增强企业获得感和满意度。
苏州西山中科药物研究开发有限公司
该公司致力于向全球客户提供全方位的药品、农药和化学品的安全评价、生态毒理检测、药效学以及药代动力学的高技术研究服务,是国内极少数具备人用药、农药和化学品GLP检测的机构。承担苏州市生物医药服务平台建设项目以及苏州市科技计划重点产业技术创新项目的研究任务,是江苏省高新技术企业、江苏省研发型企业以及江苏省农药毒理学评价和风险评估工程技术研究中心。

尤建丰走进实验室和车间,与科研人员和工作人员亲切交流,深入了解企业主营的项目和研发的具体流程。围绕企业的发展前景,尤建丰表示,企业要坚定信心、锐意创新,在擅长的领域进一步加强研究,持续推动技术进步,以更高的产品质量、更优的服务,促进企业做强做优。
2022
近日,中国食品药品检定研究院陆续发布了2022年度各项临床检验指标能力验证报告,苏州西山中科临床检验室在所参加的血液学、血凝学、尿生化和血清生化四大项共37个检测指标的能力验证活动中,均获得满意结果。这已是苏州西山中科临床检验室自2019年开始参加该能力验证活动以来,连续第四年获得同样的满分结果,这充分表明苏州西山中科临床检验室的检测能力已处于国内同行业领先水平,各项检测结果准确、可靠。

2022
为进一步提高苏州西山中科毒性病理检测服务水平,病理部诊断人员陈微、龚婷、张琼方、高飞龙、谈婷、顾玉婷和郭乾共7人参加了2022年度毒性病理检测实验室室间比对病理诊断项目考核,并在此次对比结果中荣获佳绩。
该活动由中国毒理学会毒性病理学专业委员会和广东省职业病防治院联合举办,邀请全国各大高等院校、科研机构、检测机构等参与评比。病理诊断项目考核的实验样品为SD大鼠、ICR小鼠、rasH2小鼠以及食蟹猴,涉及甲状旁腺、肾脏、视网膜、肝脏、哈氏腺、卵巢、心脏、垂体肿瘤及非肿瘤性病变共8例。
苏州西山中科病理部获得比对结果为“优秀”的考核证书,进一步证明我司病理诊断人员具备较高的诊断水平和能力,确保药物毒性评价服务的可靠和高质量。